Ifølge en gruppe forskere fra University of Pennsylvania kan kraften til sol, vind og hav snart komme sammen for å produsere miljøvennlig hydrogendrivstoff. Teamet integrerte vannrenseteknologi i et nytt eksperimentelt prosjekt sjøvann elektrolysator, som bruker en elektrisk strøm til å skille hydrogen og oksygen i vannmolekyler.
I følge Bruce Logan, professor i miljøteknikk ved Kappa og Evan Pugh University professor, kan denne nye metoden for "sjøvannssplitting" lette konverteringen av vind- og solenergi til lagringsbart og bærbart drivstoff.
"Hydrogen er et flott drivstoff, men du må få det," sa Logan. – Den eneste bærekraftige måten å gjøre dette på er å bruke fornybar energi og produsere den fra vann. Du må også bruke vann som folk ikke vil bruke til andre formål, og det ville være sjøvann. Så den hellige gral for hydrogenproduksjon måtte kombinere sjøvann, vind og solenergi som finnes i kyst- og havmiljøer."
Til tross for overflod av sjøvann, brukes det vanligvis ikke til vannseparasjon. Dersom vannet ikke avsaltes før det føres inn i elektrolysatoren – et kostbart tilleggssteg – blir klorionene i sjøvannet til giftig klorgass, som ødelegger utstyret og siver ut i miljøet.
For å forhindre dette, satte forskerne inn en tynn, semipermeabel membran som opprinnelig ble designet for å rense vann ved behandling med omvendt osmose (RO). Den omvendte osmosemembranen har erstattet ionebyttermembranen som vanligvis brukes i elektrolysatorer.
"Ideen bak omvendt osmose er at du legger veldig høyt trykk på vannet, skyver det gjennom membranen og holder klorionene bak," sa Logan.
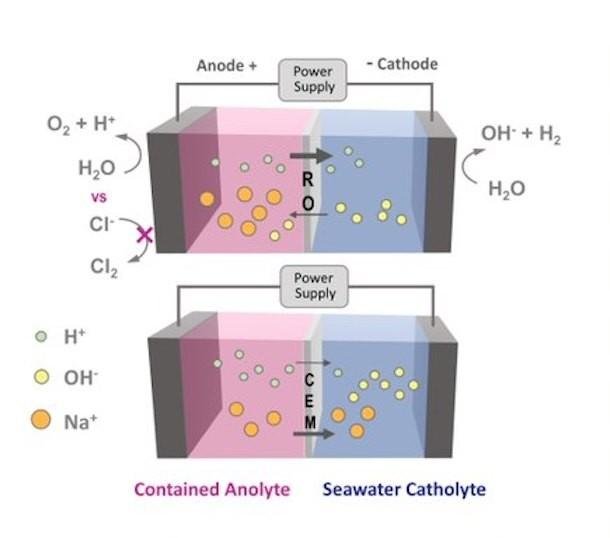
I elektrolysatoren vil sjøvann ikke lenger presse gjennom omvendt osmosemembranen, men holdes tilbake av den. Membranen brukes til å skille reaksjoner som skjer nær to neddykkede elektroder – en positivt ladet anode og en negativt ladet katode – koblet til en ekstern strømkilde. Når strømmen er slått på, begynner vannmolekyler å dele seg ved anoden, og frigjøre små hydrogenioner kalt protoner og danne oksygengass. Protonene passerer deretter gjennom membranen og kombineres med elektroner ved katoden for å danne hydrogengass.
Med en omvendt osmose-membran installert, forblir sjøvannet på katodesiden og klorionene er for store til å passere gjennom membranen og nå anoden, og forhindrer dannelsen av klorgass.
Men ved vannsplitting, som Logan påpekte, blir andre salter bevisst oppløst i vannet for å gjøre det ledende. Ionebyttermembranen, som filtrerer ioner ved elektrisk ladning, lar saltioner passere gjennom den. Det er ingen omvendt osmosemembran.
Fordi bevegelsen til større ioner er begrenset av RO-membranen, trengte forskerne å teste om de små protonene som beveget seg gjennom porene var nok til å opprettholde en høy elektrisk strøm.
I en serie eksperimenter testet forskerne to kommersielt tilgjengelige omvendt osmosemembraner og to kationbyttermembraner, en type ionebyttermembran som tillater bevegelse av alle positivt ladede ioner i systemet. Hver av dem ble testet for motstanden til membranen mot bevegelser av ioner. Mengden energi som trengs for å fullføre reaksjonene ble også beregnet, dannelsen av gassformig hydrogen og oksygen ble overvåket, interaksjonen med klorioner og skade på membranen ble analysert.
Forskerne mottok nylig et stipend på 300 000 dollar fra National Science Foundation (NSF) for å fortsette forskning på sjøvannelektrolyse. Logan håper at forskningen deres vil spille en avgjørende rolle for å redusere karbondioksidutslipp over hele verden.
Les også:
- TSMC: i 2021 vil testkopier av 3nm-prosessorer vises
- Tyngdekraften forårsaker uniformiteten til universet
